估计药物的生物利用度
在这个例子中,您将使用SimBiology™的计算参数估计能力F,药物昂丹司琼的生物利用度。您将计算F通过拟合药物的吸收和排泄模型到跟踪药物浓度随时间变化的实验数据。
这个例子需要优化工具箱™。
背景
大多数药物必须被血液吸收才能发挥作用。静脉注射(IV)药物是实现这一目标的一种方法。然而,在许多情况下,这是不切实际或不可能的。
当药物不经静脉注射时,它会通过其他途径进入血液,如通过胃肠道或口腔粘膜吸收。通过静脉给药以外的途径给药的药物通常不会被完全吸收。部分药物被直接清除,永远不会进入血液。
吸收药物的百分比是药物的生物利用度。生物利用度是药物最重要的药代动力学特性之一。它在计算非静脉给药途径的安全剂量时非常有用。生物利用度是相对于静脉给药计算的。静脉给药时,药物的生物利用度为100%其他给药途径往往会减少到达血流的药物量。
生物利用度模型
生物利用度可以使用多种方法中的一种进行建模。在本例中,您使用的模型具有胃肠道隔室和血浆隔室。口服给药由胃肠道隔室中的剂量事件建模。静脉给药由血浆隔室中的剂量事件建模。
这个例子模型药物离开GI隔在两个方面。药物可用的部分被吸收进入血液。其余部分则直接淘汰。消除的总速率,灵魂,分为吸收,卡乌中心和直接淘汰,Cl_Oral.生物利用度,F,连接彻底消除卡乌中心和Cl_Oral通过两个初始分配规则。
ka_Central = F * KA Cl_Oral =(1-F)* KA
这种药物是从消除血浆通过一级动力学隔室,在由所述参数确定的速率Cl_Central.

加载包含模型项目m1.
SBIOLADP项目(“生物利用度,sbproj”那“m1”);
数据估算生物利用度的格式
你可以通过比较不同给药条件下的患者内药物浓度来估计生物利用度。例如,病人在第一天接受静脉注射,然后在第二天接受口服剂量。在这两天,我们可以测量一段时间内药物的血浆浓度。
这些数据使我们能够估计生物利用度,以及模型的其他参数。在[2]中报告了恩丹司琼的患者时间程,在[1]中重现。
加载数据,它是一个表。
加载(“ondansetron_data.mat”);
将数据转换为分组数据对象,因为拟合函数sbiofit要求它是a分组数据对象。
GD = groupedData(ondansetron_data);
显示数据。
钆
GD = 33x5 groupedData时间药物组IV口服________ _______ _____ ___ ____ 0的NaN 1 8的NaN 0.024358 69.636 1楠楠0.087639 58.744 1楠楠0.15834 49.824 1楠楠0.38895 44.409 1楠楠0.78392 40.022 1楠楠1.3182 34.522 1楠楠1.851828.972 1楠楠2.4335 25.97 1楠楠2.9215 22.898 1楠楠3.41 20.75 1楠楠3.8744 18.095 1楠楠4.9668 13.839 1楠楠5.8962 10.876 1楠楠7.8717 6.6821 1楠楠10.01 4.0166 1楠楠12.08 2.5226 1楠楠15.2840.97816 1楠楠0的NaN 2的NaN 8 0.54951 5.3091 2楠楠0.82649 14.262 2楠楠1.0433 19.72 2楠楠1.4423 21.654 2楠楠2.0267 22.144 2楠楠2.5148 19.739 2楠楠2.9326 17.308 2楠楠3.3743 15.599 2楠楠3.955913.906 2楠楠4.9309 10.346 2楠楠6.1155 7.4489 2楠楠8.0002 5.1919 2楠楠10.091 2.9058 2楠楠12.228 1.6808 2楠楠
数据包含时间、药物浓度、分组信息、静脉注射和口服剂量等变量。第1组包含静脉注射时间过程的数据。第2组包含口服时间过程的数据。楠在药物栏中表示当时没有进行测量。楠在定量给料装置的列中的一个没有剂量通过在这个时候,路由给出。
画出口服剂量和静脉给药的药代动力学特征。
绘图(gd.时间(gd.组==1),gd.药物(gd.组==1),“标记”那“+”)举行在绘图(gd.时间(gd.组==2),gd.药物(gd.组==2),“标记”那“x”)({传奇“静脉注射8毫克”那“口服8毫克”})包含(的时间(小时)) ylabel (的浓度(毫克/升))

通知有在大约一个小时的口服剂量滞后相,而药物从胃肠道吸收进入血液。
拟合数据
估计模型的以下四个参数:
剂量舱外的总前进速率,
灵魂从
血浆隔间清除体积
血浆隔室口服药物的生物利用度,
F
设置这些参数的初始值和指定的日志变换使用的所有参数估计信息对象。
INIT = [1 1 2 0.8];estimated_parameters = estimatedInfo({'日志(KA)'那“日志(间隙)”那......‘日志(血浆)’那'分对数(F)'},“初始值”init);
因为灵魂那清除,血浆均为正物理量,对数变换反映了潜在的物理约束,并通常改善拟合。这个例子使用了一个logit转换F因为它是一个限制在0和1之间的数量。logit变换取0到1的间隔,并通过取F(治疗F作为一种可能性),对于一些药物,如茶碱,抑制F0到1之间是不合适的,因为对于具有异常吸收或代谢机制的药物,口服生物利用度可能大于1。
接下来,将响应数据映射到相应的模型组件。在该模型中,血浆药物浓度表示为血液、血浆、药物、中枢。相应的浓度数据为药物groupedData对象的变量钆.
responseMap = {“Blood_Plasma。Drug_Central= Drug'};
通过创建所需的剂量对象sbiofit处理剂量信息。首先,创建IV剂量目标Drug_Central以及口服剂量靶向Dose_Central.
iv_dose = sbiodose(“四”那“TargetName”那“Drug_Central”);口服剂量=sbiodose(“口头”那“TargetName”那'Drug_Oral');
使用这些剂量对象作为模板剂量,从剂量数据变量生成剂量对象数组四,和口头的.
适合的剂量=创建剂量(gd{“四”那“口头”},''[iv_dose,oral_dose]);
使用估计参数sbiofit.
OPTS = optimoptions(“lsqnonlin”那“显示”那“决赛”);结果= sbiofit(M1,GD,responseMap,estimated_parameters,doses_for_fit,......“lsqnonlin”,选项,[],“汇集”,真的);
当地最小的可能。lsqnonlin停止,因为在相对于其初始值的平方和最终的变化小于函数允差值。
翻译结果
首先,检查装配是否成功。
情节(结果)
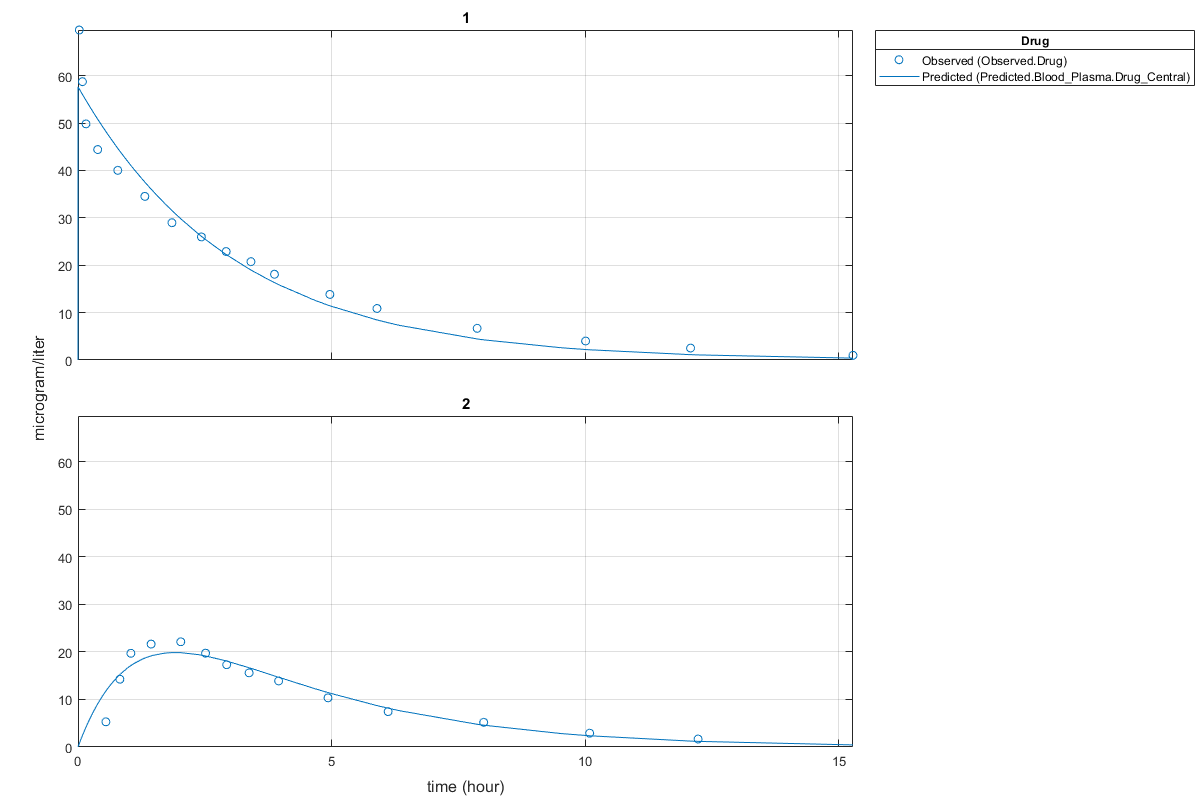
总的来说,结果似乎是一个不错的选择。然而,他们不捕获在第一时间分配阶段。这可能是可以通过增加另一个隔间提高合适,但更多的数据将被要求证明在模型的复杂性这样的增加。
当与模型拟合不满意,您可以得出关于估计参数的结论。显示存储在结果物体的参数。
results.ParameterEstimates
ans=4×3表名称StandardError的评估________________ ________ _____________ { 'KA'} 0.77947 0.1786 { '间隙'} 45.19 2.8674 { 'Blood_Plasma'} 138.73 4.5249 { 'F'} 0.64455 0.066013
的参数F是的生物利用度。结果表明,昂丹司琼具有大约64%的生物利用率。这一估计符合文献报道,在2-24毫克范围昂丹司琼的口服给药具有60%的生物利用度[1,2]。
血浆是分配的体积。这个结果是合理地接近160升Vd的报道昂丹司琼[1]。所估计的间隙为45.4升/小时。
灵魂不直接映射到一个广泛报道的药代动力学参数。从两个角度考虑。我们可以说64%的药物是可用的,并且可用的药物具有0.4905/HR的吸收参数。或者,可以说从GI室的药物清除率是0.7402/HR,而从胃肠道清除的药物的64%是ABSO。血液中有红细胞。
推广这种方法
lsqnonlin,以及其他一些优化算法支持金宝appsbiofit,是局部算法。局部算法有可能在所有可能的参数选择中找到不是最佳结果的结果。由于局部算法不能保证收敛到全局最佳拟合,因此在拟合PK模型时,使用不同的初始条件多次重新开始拟合是一种很好的做法。或者,sbiofit金宝app支持多种全局方法,如粒子群或遗传算法优化。在从参数的值得出结论之前,验证一个拟合的质量是一个重要的步骤。
此示例使用的数据是多个患者的平均时间过程。当使用来自更多患者的数据拟合模型时,患者之间的某些参数可能相同,有些则不同。此类要求引入了分层建模的需要。您可以通过配置CategoryVariableName旗估计信息对象。
参考文献
《昂丹司琼临床药代动力学》,《临床药代动力学》29.2(1995):95-109。
科瑟普,P. V.和J. L.帕尔默。昂丹西酮的血浆和药代动力学测定欧洲癌症与临床肿瘤学杂志25 (1988):S71-4。

